Энергия — скалярная физическая величина, являющаяся единой мерой различных форм движения материи и мерой перехода движения материи из одних форм в другие. Существует довольно много форм энергии: Механика различает потенциальную энергию (или, в более общем случае, энергия взаимодействия тел или их частей) и кинетическую энергию (энергия движения). Их сумма называется полной энергией. Энергией обладают все виды полей. По этому признаку различают: электрическую (электромагнитную), гравитационную и ядерную энергии. В химии рассматриваются такие величины как энергия связи. Тепловая энергия — энергия хаотического движения молекул.
Термодинамика основывается на трёх законах, которые сформулированы на основе экспериментальных данных и поэтому могут быть приняты как постулаты.
Первый закон термодинамики представляет собой формулировку обобщённого закона сохранения энергии для термодинамических процессов. В наиболее простой форме его можно записать как:
$$\mathrm{d}Q = \mathrm{d}U + \mathrm{d}A,$$где $\mathrm{d}U$ есть полный дифференциал внутренней энергии системы, а $\mathrm{d}Q$ и $\mathrm{d}A$ есть элементарное количество теплоты и элементарная работа, совершенная над системой соответственно.
Термодинамический подход к изучению молекулярных систем заключается в том, что состояние молекулярной системы определяется через изменение ее внутренней энергии. Первое начало термодинамики утверждает: внутреннюю энергию молекулярной системы можно изменить либо в процессе совершения работы, либо в процессе теплопередачи. Возьмем жидкостный U-образный манометр, на одном колене которого укреплен теплоприемник, а другое открыто. Накроем теплоприемник платком (чтобы тепло от руки не передавалось теплоприемнику) и будем оказывать на него давление рукой. Деформируя теплоприемник, мы изменяем давление газа и, следовательно, изменяем внутреннюю энергию газа в теплоприемнике. Газ, в свою очередь, совершает работу над столбом жидкости и поднимает его уровень в свободном колене. Осветим теплоприемник светом от настольной лампы. Тепловое излучение лампы будет поглощаться теплоприемником, и это приведет к нагреванию газа, то есть к изменению его внутренней энергии. Газ, в свою очередь, совершит работу над столбом жидкости и поднимет уровень жидкости в открытом колене манометра.
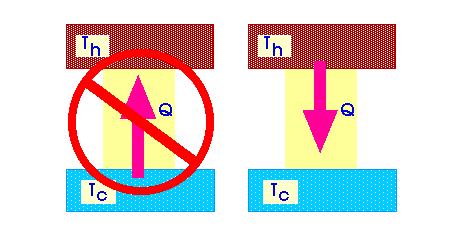
Второй закон термодинамики исключает возможность создания вечного двигателя. Имеется несколько различных, но в тоже время эквивалентных формулировок этого закона. Постулат Клаузиуса. Процесс, при котором не происходит других изменений, кроме передачи теплоты от горячего тела к холодному, является необратимым, то есть теплота не может перейти от холодного тела к горячему без каких либо других изменений в системе. Это явление называют рассеиванием или дисперсией энергии.
Постулат Кельвина. Процесс, при котором работа переходит в теплоту без каких либо других изменений в системе, является необратимым, то есть невозможно превратить в работу всю теплоту, взятую от источника с однородной температурой, не проводя других изменений в системе.
Второй закон термодинамики можно сформулировать следующим образом: "Периодически работающая тепловая машина должна иметь три части: нагреватель, рабочее тело и холодильник". Рабочее тело получает тепло от нагревателя, часть тепла переводит в механическую работу, а часть выбрасывает в холодильник. Опыт Дарлинга - это модель тепловой машины. На дно стакана наливаем анилин, сверху добавляем воду и помещаем стакан на плитку. При комнатной температуре плотность анилина больше плотности воды и он находится под водой. При температуре выше 60 С плотность анилина становится меньше плотности воды и анилин всплывает вверх. Вверху анилин отдает тепло окружающему воздуху, охлаждается и тонет. Таким образом, мы имеем: нагреватель - плитка, холодильник - воздух в верхней части стакана, рабочее тело - анилин. Анилин, получив тепловую энергию от плитки, совершает работу по подъему самого себя вверх, часть энергии сбрасывает в холодильник, охлаждается.
Теорема Нернста: Энтропия любой системы при абсолютном нуле температуры всегда может быть принята равной нулю.
В конце небольшая информация к размышлению: 2-й Закон однозначно запрещает эволюцию. Живые организмы состоят из тех же атомов и молекул, из которых состоит и любая термодинамическая система, и поэтому на них также должен распространяться 2-й Закон. Если взять в качестве примера груду кирпичей, то с течением времени каждый кирпич превратится в пыль. Куча этих кирпичей самопроизвольно не может становится домом! Это очевидный абсурд. Эволюция, то есть, саморазвитие материи “от простого к сложному” абсолютно запрещена 2-м Законом термодинамики. Также, закон природы, утверждающий, что материя непрерывно распадается, причем увеличивается беспорядок Вселенной и теряется теплота, уже давно порицается христианскими фундаменталистами как очевидное противоречие их догматам божественного милосердия и вечного спасения. Однако 2-й Закон термодинамики с полным правом может быть назван “научным евангелием” – ибо из него следует совершенно однозначный вывод о существовании Бога, сотворившего мир.
